เยื่อหุ้มนิวเคลียส
เยื่อหุ้มนิวเคลียส (อังกฤษ: Nuclear envelope, perinuclear envelope, nuclear membrane, nucleolemma หรือ karyotheca)[1][2][3] เป็นชั้นของลิพิดไบเลเยอร์ (lipid bilayer) ในเซลล์ยูแคริโอต ซึ่งทำหน้าที่ห่อหุ้มนิวเคลียสของเซลล์ที่ห่อหุ้มสารพันธุกรรม
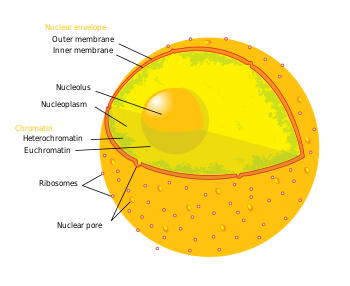
เยื่อหุ้มนิวเคลียสประกอบด้วยเยื่อหุ้มสองชั้นที่สร้างจากชั้นไขมันสองชั้น (Lipid bilayer membrane) ได้แก่ เยื่อหุ้มด้านในของนิวเคลียส (Inner nuclear membrane) และเยื่อหุ้มด้านนอกของนิวเคลียส (Outer nuclear membrane)[4] พื้นที่ระหว่างเยื่อหุ้มทั้งสองเรียกว่า ช่องว่างระหว่างเยื่อหุ้มนิวเคลียส (Perinuclear space) ซึ่งโดยปกติจะมีความกว้างประมาณ 10–50 นาโนเมตร[5][6] โดยเยื่อหุ้มด้านนอกนั้นมีการเชื่อมต่อกับเยื่อหุ้มของเอนโดพลาสมิกเรติคูลัม (Endoplasmic reticulum)[4] นอกจากนี้เยื่อหุ้มนิวเคลียสยังมีรูพรุนจำนวนมากที่เรียกว่ารูพรุนของนิวเคลียส (Nuclear pores) ซึ่งช่วยให้วัตถุต่าง ๆ เคลื่อนที่ระหว่างไซโทซอล (Cytosol) และนิวเคลียสได้[4] นอกจากนี้ยังมีโปรตีนในกลุ่มอินเทอร์มีเดียท ฟิลาเมนท์ (Intermediate filament) ที่เรียกว่าลามิน(Lamin) ที่รวมตัวกันสร้างโครงสร้างที่เรียกว่านิวเคลียร์ลามินา (Nuclear lamina) ซึ่งอยู่ภายในของเยื่อหุ้มด้านในของนิวเคลียส โดยโครงสร้างนี้มีหน้าที่ในการค้ำจุนเชิงโครงสร้างให้แก่นิวเคลียส[4]
โครงสร้าง
[แก้]เยื่อหุ้มนิวเคลียสประกอบด้วยเยื่อหุ้มสองชั้นที่สร้างจากเยื่อไขมันสองชั้น ได้แก่เยื่อหุ้มนิวเคลียสด้านใน และเยื่อหุ้มนิวเคลียสด้านนอก เยื่อหุ้มทั้งสองนี้เชื่อมต่อกันด้วยรูพรุนของนิวเคลียส เยื่อหุ้มนิวเคลียสได้รับการค้ำจุนโครงสร้างโดยอินเทอร์มีเดียท ฟิลาเมนท์สองชุด โดยชุดแรกได้ก่อตัวเป็นโครงข่ายภายในที่เรียกว่านิวเคลียร์ลามินาอยู่บริเวณเยื่อหุ้มด้านใน[7] ส่วนอีกชุดหนึ่งก่อตัวเป็นโครงข่ายที่หลวมกว่า ณ บริเวณด้านนอกเพื่อค้ำจุนโครงสร้างจากภายนอก[4] รูปร่างของเยื่อหุ้มนิวเคลียสโดยแท้จริงนั้นไม่มีรูปร่างที่แน่นอน (Irregular) โดยมีการยื่นยืดหดอย่างสม่ำเสมอ ซึ่งสามารถสังเกตได้ผ่านกล้องจุลทรรศน์อิเล็กตรอน

เยื่อหุ้มชั้นนอก
[แก้]เยื่อหุ้มนิวเคลียสชั้นนอกนั้นมีขอบเขตที่ใช้ร่วมกับเอนโดพลาสมิกเรติคูลัม[8] แต่ถึงแม้ว่าจะมีการเชื่อมต่อทางกายภาพซึ่งกันและกัน แต่เยื่อหุ้มด้านนอกของนิวเคลียสมีโปรตีนในความเข้มข้นที่สูงกว่าเยื่อหุ้มของเอนโดพลาสมิกเรติคูลัมเป็นอย่างมาก[9] โปรตีนเนสพริน (Nesprin - Nuclear envelope spectrin repeat proteins) ทั้งสี่ชนิดที่พบในสัตว์เลี้ยงลูกด้วยนมนั้นมีปรากฏอยู่ในเยื่อหุ้มด้านนอกของนิวเคลียส[10] โดยเนสปรินทำหน้าที่เชื่อมต่อเส้นใยโครงร่างของเซลล์ (Cytoskeletal filaments) เข้ากับโครงร่างของนิวเคลียส (Nucleoskeleton)[11] การเชื่อมต่อที่อาศัยเนสปรินกับโครงร่างเซลล์นี้มีบทบาทในการกำหนดตำแหน่งของนิวเคลียสและในหน้าที่การรับรู้เชิงกลของเซลล์[12] โปรตีนในกลุ่ม KASH domain ของเนสปริน-1 และเนสปริน-2 เป็นส่วนหนึ่งของโครงสร้าง LINC complex (Linker of nucleoskeleton and cytoskeleton) ซึ่งสามารถจับกับองค์ประกอบของโครงร่างเซลล์ได้โดยตรง เช่น เส้นใยแอคตินหรือจับกับโปรตีนในช่องว่างระหว่างเยื่อหุ้มนิวเคลียสได้เช่นกัน[13][14] สำหรับเนสปริน-3 และเนสปริน-4 นั้นอาจมีบทบาทในการขนถ่ายวัตถุขนาดใหญ่ โดยเนสปริน-3 เชื่อมต่อกับโปรตีนเพล็คติน และเชื่อมต่อเยื่อหุ้มนิวเคลียสกับเส้นใยอินเทอร์มีเดียท ฟิลาเมนท์ในไซโทพลาซึม[15] ในขณะที่เนสปริน-4 เชื่อมต่อกับโปรตีนไคเนซิน-1 (Kinesin-1) ซึ่งเป็นโปรตีนขนส่ง[16] นอกจากนี้ เยื่อหุ้มนิวเคลียสด้านนอกยังมีบทบาทในกระบวนการพัฒนาโดยการหลอมรวมเข้ากับเยื่อหุ้มด้านในเพื่อสร้างรูพรุนของนิวเคลียส[17]
เยื่อหุ้มชั้นใน
[แก้]อ่านเพิ่มเติม: โปรตีนของเยื่อหุ้มนิวเคลียสชั้นใน
เยื่อหุ้มนิวเคลียสด้านในทำหน้าที่ห่อหุ้มนิวคลีโอพลาสซึม (Nucleoplasm) และถูกปกคลุมด้วยนิวเคลียร์ลามินา ซึ่งเป็นโครงตาข่ายของอินเทอร์มีเดียท ฟิลาเมนท์ที่ช่วยเสริมความมั่นคงให้กับเยื่อหุ้มนิวเคลียส รวมถึงมีบทบาทในการทำงานของโครมาติน[9] เยื่อหุ้มด้านในเชื่อมต่อกับเยื่อหุ้มด้านนอกผ่านรูพรุนของนิวเคลียส ซึ่งเจาะทะลุผ่านเยื่อหุ้มทั้งสอง แม้ว่าเยื่อหุ้มทั้งสองและเอนโดพลาสมิกเรติคูลัมจะเชื่อมต่อกัน แต่โปรตีนที่ฝังตัวอยู่ในเยื่อหุ้มมักจะคงอยู่ในตำแหน่งเดิมแทนที่จะกระจายตัวไปตามเครือข่ายที่เชื่อมต่อกัน[18] นอกจากนี้ เยื่อหุ้มด้านในยังประกอบด้วยเครือข่ายเส้นใยที่เรียกว่านิวเคลียร์ลามินา ซึ่งมีความหนาประมาณ 10–40 นาโนเมตร และมีบทบาทสำคัญในการเสริมความแข็งแรงให้กับเยื่อหุ้มนิวเคลียส
การกลายพันธุ์ในยีนที่เกี่ยวข้องในการเข้ารหัสโปรตีนของเยื่อหุ้มนิวเคลียสด้านในสามารถก่อให้เกิดโรคในกลุ่มลามิโนพาธี (Laminopathy) ได้
รูพรุนของนิวเคลียส
[แก้]บทความหลัก: รูพรุนของนิวเคลียส

เยื่อหุ้มนิวเคลียสนั้นมีรูพรุนประมาณหนึ่งพันรู ซึ่งถูกเจาะเป็นรูโดยโครงสร้างรูพรุนของนิวเคลียส (Nuclear pore complexes) โดยแต่ละโครงสร้างมีขนาดประมาณ 100 นาโนเมตร และมีช่องด้านในที่กว้างประมาณ 40 นาโนเมตร[9] โครงสร้างเหล่านี้ประกอบด้วยโปรตีนที่เรียกว่านิวคลีโอพอริน (Nucleoporin) ซึ่งทำหน้าที่เชื่อมโยงเยื่อหุ้มด้านในและเยื่อหุ้มด้านนอกของนิวเคลียสเข้าด้วยกัน
การแบ่งเซลล์
[แก้]ในระยะ G2 ซึ่งเป็นระยะย่อยของระยะอินเตอร์เฟส (interphase) เยื่อหุ้มนิวเคลียสจะเพิ่มพื้นที่ผิวและเพิ่มจำนวนรูพรุนของนิวเคลียสเป็นสองเท่า[9] ซึ่งในสิ่งมีชีวิตยูคาริโอต เช่น ยีสต์ (Yeast) ที่มีการแบ่งเซลล์แบบไมโทซิสแบบปิด (Closed mitosis) นั้นเยื่อหุ้มนิวเคลียสจะยังคงอยู่ในสภาพเดิมตลอดกระบวนการแบ่งเซลล์ ในการแบ่งเซลล์นั้นเส้นใยสปินเดิล (Spindle fibers) อาจก่อตัวขึ้นภายในเยื่อหุ้ม หรือเจาะทะลุผ่านเยื่อหุ้มโดยไม่ทำให้มันฉีกขาด[9] ในยูคาริโอตชนิดอื่น เช่น สัตว์และพืช เยื่อหุ้มนิวเคลียสจำเป็นต้องสลายตัวในระยะโพรเมทาเฟส (Prometaphase) ของการแบ่งเซลล์แบบไมโทซิส เพื่อให้เส้นใยสปินเดิลเข้าถึงโครโมโซมที่อยู่ภายในได้ อย่างไรก็ตาม กระบวนการสลายตัวและการสร้างใหม่ของเยื่อหุ้มนิวเคลียสยังไม่ได้รับการศึกษาจนเข้าใจได้อย่างสมบูรณ์
การสลายตัว
[แก้]
ในสัตว์เลี้ยงลูกด้วยนมนั้นเยื่อหุ้มนิวเคลียสสามารถสลายตัวภายในเวลาไม่กี่นาที โดยเป็นไปตามลำดับขั้นตอนในระยะเริ่มต้นของกระบวนการทางไมโทซิส ขั้นแรก M-Cdk จะทำการเชื่อมโลเลกุลกลุ่มฟอสเฟต (Phosphorylate) เข้ากับพอลิเพปไทด์ของนิวคลีโอพอริน และพวกมันบางส่วนจะถูกคัดเลือกเพื่อนำออกจากโครงสร้างรูพรุนของนิวเคลียสอย่างเฉพาะเจาะจง หลังจากนั้น โครงสร้างรูพรุนของนิวเคลียสที่เหลือจะสลายตัวพร้อมกัน หลักฐานทางชีวเคมีได้แสดงให้เห็นว่าโครงสร้างรูพรุนของนิวเคลียสจะสลายตัวเป็นชิ้นส่วนที่เสถียรแทนที่จะสลายเป็นชิ้นส่วนขนาดเล็กของพอลิเพปไทด์[9] นอกจากนี้ M-Cdk ยังทำการเชื่อมต่อกลุ่มฟอสเฟตเข้ากับองค์ประกอบของแผ่นนิวเคลียร์ลามินาซึ่งเป็นโครงสร้างที่ค้ำจุนเยื่อหุ้มนิวเคลียสอีกด้วย ส่งผลให้นิวเคลียร์ลามินาสลายตัว และเยื่อหุ้มนิวเคลียสแยกออกเป็นถุงเวสิเคิลขนาดเล็ก[19] ภาพถ่ายจากกล้องจุลทรรศน์อิเล็กตรอนและกล้องจุลทรรศน์ฟลูออเรสเซนส์ให้หลักฐานที่ชัดเจนว่าเยื่อหุ้มนิวเคลียสถูกดูดซึมโดยเอนโดพลาสมิกเรติคูลัม ทั้งนี้เนื่องจากมีการพบโปรตีนในนิวเคลียสที่ในสภาวะปกตินั้นไม่ได้ปรากฏอยู่ในเอนโดพลาสมิกเรติคูลัมเกิดขึ้นในระหว่างการแบ่งเซลล์แบบไมโทซิส[9]
นอกจากการสลายตัวของเยื่อหุ้มนิวเคลียสในระยะโพรเมทาเฟสของการแบ่งเซลล์แบบไมโทซิสแล้ว เยื่อหุ้มนิวเคลียสยังสามารถเกิดการแตกออกมาได้ในเซลล์สัตว์เลี้ยงลูกด้วยนมที่เคลื่อนที่ (Migrating cells) ในระยะอินเตอร์เฟสของวัฏจักรเซลล์ (Cell cycle)[20] การแตกออกมานี้เกิดขึ้นชั่วคราว และมีแนวโน้มว่าเป็นผลจากการเปลี่ยนรูปของนิวเคลียส
กระบวนการซ่อมแซมเยื่อหุ้มนิวเคลียสที่แตกออกนี้เกิดขึ้นอย่างรวดเร็ว โดยอาศัยกลไกที่ขึ้นอยู่กับโครงสร้างคัดแยกเอนโดโซมที่จำเป็นต่อการขนส่ง (Endosomal Sorting Complexes Required for Transport - ESCRT) ซึ่งประกอบด้วยโปรตีนเชิงซ้อนในไซโทซอล[20] นอกจากนี้ในระหว่างที่เยื่อหุ้มนิวเคลียสแตกออกย่อมเกิดความเสียหายแก่ดีเอ็นเอเกลียวคู่แบบขาดออกจากกันได้
ด้วยเหตุนี้ ความสามารถของเซลล์ในการเอาตัวรอดเมื่อต้องเคลื่อนที่ผ่านสภาพแวดล้อมที่คับแคบนั้นดูเหมือนว่าจะขึ้นอยู่กับประสิทธิภาพของกลไกซ่อมแซมเยื่อหุ้มนิวเคลียสและดีเอ็นเอ
การสลายตัวของเยื่อหุ้มนิวเคลียสที่ผิดปกติถูกพบในโรคกลุ่มลามิโนพาธีและในเซลล์มะเร็ง ซึ่งส่งผลให้เกิดการกระจายตัวผิดตำแหน่งของโปรตีนภายในเซลล์ อันนำมาซึ่งการเกิดไมโครนิวเคลียส (Micronucleus) และความไม่เสถียรของจีโนม[21][22][23]
การสร้างใหม่
[แก้]กระบวนการที่เยื่อหุ้มนิวเคลียสถูกสร้างขึ้นใหม่ในระยะเทโลเฟสของการแบ่งเซลล์แบบไมโทซิสนั้นยังคงเป็นหัวข้อที่มีการถกเถียงกันอยู่ โดยมีสองทฤษฎีหลักที่เสนอไว้[9] ได้แก่
- การหลอมรวมของถุงเวสิเคิล ถุงเวสิเคิลที่ประกอบด้วยเยื่อหุ้มนิวเคลียสจะหลอมรวมกันเพื่อสร้างเยื่อหุ้มนิวเคลียสขึ้นใหม่
- การปรับรูปร่างของเอนโดพลาสมิกเรติคูลัม ชิ้นส่วนของเอนโดพลาสมิกเรติคูลัมที่ดูดซับเยื่อหุ้มนิวเคลียสไว้จะห่อหุ้มพื้นที่นิวเคลียส และสร้างเยื่อหุ้มนิวเคลียสที่ปิดสนิทขึ้นใหม่
ต้นกำเนิดของเยื่อหุ้มนิวเคลียส
[แก้]การศึกษาเปรียบเทียบจีโนม, วิวัฒนาการ และต้นกำเนิดของเยื่อหุ้มนิวเคลียสนำไปสู่ข้อเสนอว่านิวเคลียสเกิดขึ้นในบรรพบุรุษยูคาริโอตดั้งเดิมหรือที่เรียกว่า “พรีคาริโอต” (Prekaryote) ซึ่งถูกกระตุ้นโดยความสัมพันธ์แบบอิงอาศัยระหว่างอาร์เคียและแบคทีเรีย[24] มีแนวคิดหลายประการที่อธิบายถึงต้นกำเนิดเชิงวิวัฒนาการของเยื่อหุ้มนิวเคลียส[25] เช่น การเว้าของเยื่อหุ้มเซลล์ (Plasma membrane) ในบรรพบุรุษโปรคาริโอต หรือการสร้างระบบเยื่อหุ้มใหม่หลังจากการก่อตัวของไมโทคอนเดรียดั้งเดิม (Proto-mitochondria) ในเซลล์เจ้าบ้านที่เป็นอาร์เคีย หนึ่งในความสามารถทางการปรับตัวที่สำคัญของเยื่อหุ้มนิวเคลียสอาจเป็นการทำหน้าที่เป็นเกราะป้องกันจีโนมจากอนุมูลออกซิเจน (Reactive oxygen species - ROS) ซึ่งถูกสร้างขึ้นโดยไมโทคอนเดรียดั้งเดิมของเซลล์ในยุคนั้น[26][27]
แหล่งข้อมูลอื่น
[แก้]- ภาพเนื้อเยื่อจากมหาวิทยาลัยบอสตัน 20102loa (อังกฤษ)
- Animations of nuclear pores and transport through the nuclear envelope เก็บถาวร 2009-02-07 ที่ เวย์แบ็กแมชชีน
- Illustrations of nuclear pores and transport through the nuclear envelope เก็บถาวร 2009-02-07 ที่ เวย์แบ็กแมชชีน
อ้างอิง
[แก้]- ↑ "Cell Nucleus and Nuclear Envelope". web.archive.org. 2018-06-18. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2018-06-18. สืบค้นเมื่อ 2025-01-01.
{{cite web}}: CS1 maint: bot: original URL status unknown (ลิงก์) - ↑ "Nuclear envelope". Biology Articles, Tutorials & Dictionary Online (ภาษาอังกฤษแบบอเมริกัน). 2019-10-07.
- ↑ "Definition of NUCLEAR MEMBRANE". www.merriam-webster.com (ภาษาอังกฤษ). 2024-11-22.
- ↑ 4.0 4.1 4.2 4.3 4.4 Alberts, Bruce, บ.ก. (2002). Molecular biology of the cell (4th ed ed.). New York: Garland Science. ISBN 978-0-8153-4072-0.
{{cite book}}:|edition=has extra text (help) - ↑ "Perinuclear space - Definition and Examples - Biology Online Dictionary". Biology Articles, Tutorials & Dictionary Online (ภาษาอังกฤษแบบอเมริกัน). 2020-11-09.
- ↑ Berrios, Miguel (1998). Nuclear structure and function. Methods in cell biology. San Diego: Academic Press. ISBN 978-0-12-564155-5.
- ↑ Coutinho, Henrique Douglas M; Falcão-Silva, Vivyanne S; Gonçalves, Gregório Fernandes; da Nóbrega, Raphael Batista (2009-04-20). "Molecular ageing in progeroid syndromes: Hutchinson-Gilford progeria syndrome as a model". Immunity & Ageing (ภาษาอังกฤษ). 6 (1). doi:10.1186/1742-4933-6-4. ISSN 1742-4933.
- ↑ "Chloride channels in the Nuclear membrane" (PDF). Harvard.edu. Archived from the original (PDF) on 2 August 2010. Retrieved 7 December 2012.
- ↑ 9.0 9.1 9.2 9.3 9.4 9.5 9.6 9.7 Hetzer, Martin W (2010 Mar). "The Nuclear Envelope". Cold Spring Harbor Perspectives in Biology (ภาษาอังกฤษ). 2 (3). doi:10.1101/c.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Wilson, Katherine L.; Berk, Jason M. (2010-06-15). "The nuclear envelope at a glance". Journal of Cell Science (ภาษาอังกฤษ). 123 (12): 1973–1978. doi:10.1242/jcs.019042. ISSN 1477-9137. PMC 2880010. PMID 20519579.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Burke, Brian; Roux, Kyle J. (2009-11). "Nuclei Take a Position: Managing Nuclear Location". Developmental Cell (ภาษาอังกฤษ). 17 (5): 587–597. doi:10.1016/j.devcel.2009.10.018.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Uzer, Gunes; Thompson, William R; Sen, Buer; Xie, Zhihui; Yen, Sherwin S; Miller, Sean; Bas, Guniz; Styner, Maya; Rubin, Clinton T; Judex, Stefan; Burridge, Keith (2015 Jun). "Cell Mechanosensitivity to Extremely Low Magnitude Signals is Enabled by a LINCed Nucleus". Stem cells (Dayton, Ohio) (ภาษาอังกฤษ). 33 (6). doi:10.1002/.
{{cite journal}}: ตรวจสอบค่า|doi=(help); ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Crisp, Melissa; Liu, Qian; Roux, Kyle; Rattner, J.B.; Shanahan, Catherine; Burke, Brian; Stahl, Phillip D.; Hodzic, Didier (2006-01-02). "Coupling of the nucleus and cytoplasm: Role of the LINC complex". The Journal of Cell Biology (ภาษาอังกฤษ). 172 (1): 41–53. doi:10.1083/jcb.200509124. ISSN 1540-8140. PMC 2063530. PMID 16380439.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Zeng, Xinhua; Li, Keqi; Yuan, Rong; Gao, Hongfei; Luo, Junling; Liu, Fang; Wu, Yuhua; Wu, Gang; Yan, Xiaohong (2018-01-09). "Nuclear Envelope-Associated Chromosome Dynamics during Meiotic Prophase I". Frontiers in Cell and Developmental Biology. 5. doi:10.3389/fcell.2017.00121. ISSN 2296-634X. PMC 5767173. PMID 29376050.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Wilhelmsen, Kevin; Litjens, Sandy H.M.; Kuikman, Ingrid; Tshimbalanga, Ntambua; Janssen, Hans; van den Bout, Iman; Raymond, Karine; Sonnenberg, Arnoud (2005-12-05). "Nesprin-3, a novel outer nuclear membrane protein, associates with the cytoskeletal linker protein plectin". The Journal of Cell Biology (ภาษาอังกฤษ). 171 (5): 799–810. doi:10.1083/jcb.200506083. ISSN 1540-8140. PMC 2171291. PMID 16330710.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Roux, Kyle J.; Crisp, Melissa L.; Liu, Qian; Kim, Daein; Kozlov, Serguei; Stewart, Colin L.; Burke, Brian (2009-02-17). "Nesprin 4 is an outer nuclear membrane protein that can induce kinesin-mediated cell polarization". Proceedings of the National Academy of Sciences (ภาษาอังกฤษ). 106 (7): 2194–2199. doi:10.1073/pnas.0808602106. ISSN 0027-8424. PMC 2650131. PMID 19164528.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Fichtman, Boris; Ramos, Corinne; Rasala, Beth; Harel, Amnon; Forbes, Douglass J. (2010-12). Weis, Karsten (บ.ก.). "Inner/Outer Nuclear Membrane Fusion in Nuclear Pore Assembly: Biochemical Demonstration and Molecular Analysis". Molecular Biology of the Cell (ภาษาอังกฤษ). 21 (23): 4197–4211. doi:10.1091/mbc.e10-04-0309. ISSN 1059-1524. PMC 2993748. PMID 20926687.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help)CS1 maint: PMC format (ลิงก์) - ↑ Georgatos, S. D. (2001-06-15). "NEW EMBO MEMBER'S REVIEW: The inner nuclear membrane: simple, or very complex?". The EMBO Journal. 20 (12): 2989–2994. doi:10.1093/emboj/20.12.2989. PMC 150211. PMID 11406575.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Alberts, Bruce; Wilson, John H.; Hunt, Tim; Johnson, Alexander, บ.ก. (2008). Molecular biology of the cell: media DVD-ROM inside (5. ed ed.). New York, NY: Garland Science. ISBN 978-0-8153-4106-2.
{{cite book}}:|edition=has extra text (help) - ↑ 20.0 20.1 Raab, Matthew; Gentili, Matteo; de Belly, Henry; Thiam, Hawa-Racine; Vargas, Pablo; Jimenez, Ana Joaquina; Lautenschlaeger, Franziska; Voituriez, Raphaël; Lennon-Duménil, Ana-Maria; Manel, Nicolas; Piel, Matthieu (2016-04-15). "ESCRT III repairs nuclear envelope ruptures during cell migration to limit DNA damage and cell death". Science (ภาษาอังกฤษ). 352 (6283): 359–362. doi:10.1126/science.aad7611. ISSN 0036-8075.
- ↑ Vargas, Jesse D.; Hatch, Emily M.; Anderson, Daniel J.; Hetzer, Martin W. (2012-01). "Transient nuclear envelope rupturing during interphase in human cancer cells". Nucleus (ภาษาอังกฤษ). 3 (1): 88–100. doi:10.4161/nucl.18954. ISSN 1949-1034. PMC 3342953. PMID 22567193.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help)CS1 maint: PMC format (ลิงก์) - ↑ Lim, Sanghee; Quinton, Ryan J.; Ganem, Neil J. (2016-11). Bement, William (บ.ก.). "Nuclear envelope rupture drives genome instability in cancer". Molecular Biology of the Cell (ภาษาอังกฤษ). 27 (21): 3210–3213. doi:10.1091/mbc.E16-02-0098. ISSN 1059-1524. PMC 5170854. PMID 27799497.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help)CS1 maint: PMC format (ลิงก์) - ↑ Hatch, Emily M.; Hetzer, Martin W. (2016-10-10). "Nuclear envelope rupture is induced by actin-based nucleus confinement". Journal of Cell Biology (ภาษาอังกฤษ). 215 (1): 27–36. doi:10.1083/jcb.201603053. ISSN 0021-9525. PMC 5057282. PMID 27697922.
{{cite journal}}: CS1 maint: PMC format (ลิงก์) - ↑ Mans, Berend; Anantharaman, Vivek; Aravind, L.; Koonin, Eugene V. (2004-12). "Comparative Genomics, Evolution and Origins of the Nuclear Envelope and Nuclear Pore Complex". Cell Cycle (ภาษาอังกฤษ). 3 (12): 1625–1650. doi:10.4161/cc.3.12.1316. ISSN 1538-4101.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Martin, William (2005-12). "Archaebacteria (Archaea) and the origin of the eukaryotic nucleus". Current Opinion in Microbiology (ภาษาอังกฤษ). 8 (6): 630–637. doi:10.1016/j.mib.2005.10.004.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Speijer, Dave (2015-12). "Birth of the eukaryotes by a set of reactive innovations: New insights force us to relinquish gradual models". BioEssays (ภาษาอังกฤษ). 37 (12): 1268–1276. doi:10.1002/bies.201500107. ISSN 0265-9247.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Witzany, Guenther, บ.ก. (2017). Biocommunication of Archaea (ภาษาอังกฤษ). Cham: Springer International Publishing. doi:10.1007/978-3-319-65536-9. ISBN 978-3-319-65535-2.
