รายชื่อสถานะออกซิเดชันของธาตุ
หน้าตา
ด้านล่างนี้เป็นรายชื่อสถานะออกซิเดชันของธาตุ
รายชื่อ
[แก้] ธาตุ
แก๊สมีสกุล
| ธาตุ | สถานะ ออกซิเดชัน เป็นลบ |
ศูนย์ | สถานะ ออกซิเดชัน เป็นบวก |
หมายเหตุ | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| −4 | −3 | −2 | −1 | 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | ||
| ไฮโดรเจน | −1 | H | +1 | |||||||||||
| ฮีเลียม | He | |||||||||||||
| ลิเทียม | Li | +1 | ||||||||||||
| เบริลเลียม | Be | +1 | +2 | [1] | ||||||||||
| โบรอน | B | +1 | +2 | +3 | ||||||||||
| คาร์บอน | −4 | −3 | −2 | −1 | C | +1 | +2 | +3 | +4 | |||||
| ไนโตรเจน | −3 | −2 | −1 | N | +1 | +2 | +3 | +4 | +5 | |||||
| ออกซิเจน | −2 | −1 | O | +1 | +2 | |||||||||
| ฟลูออรีน | −1 | F | ||||||||||||
| นีออน | Ne | |||||||||||||
| โซเดียม | −1 | Na | +1 | |||||||||||
| แมกนีเซียม | Mg | +1 | +2 | [2] | ||||||||||
| อะลูมิเนียม | Al | +1 | +2 | +3 | [3] | |||||||||
| ซิลิคอน | −4 | −3 | −2 | −1 | Si | +1 | +2 | +3 | +4 | |||||
| ฟอสฟอรัส | −3 | −2 | −1 | P | +1 | +2 | +3 | +4 | +5 | |||||
| กำมะถัน | −2 | −1 | S | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| คลอรีน | −1 | Cl | +1 | +2 | +3 | +4 | +5 | +6 | +7 | |||||
| อาร์กอน | Ar | |||||||||||||
| โพแทสเซียม | −1 | K | +1 | |||||||||||
| แคลเซียม | Ca | +1 | +2 | [4] | ||||||||||
| สแกนเดียม | Sc | +1 | +2 | +3 | ||||||||||
| ไทเทเนียม | −1 | Ti | +1 | +2 | +3 | +4 | [5] | |||||||
| วาเนเดียม | −1 | V | +1 | +2 | +3 | +4 | +5 | |||||||
| โครเมียม | −2 | −1 | Cr | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| แมงกานีส | −3 | −2 | −1 | Mn | +1 | +2 | +3 | +4 | +5 | +6 | +7 | |||
| เหล็ก | −2 | −1 | Fe | +1 | +2 | +3 | +4 | +5 | +6 | [6] | ||||
| โคบอลต์ | −1 | Co | +1 | +2 | +3 | +4 | +5 | |||||||
| นิกเกิล | −1 | Ni | +1 | +2 | +3 | +4 | ||||||||
| ทองแดง | Cu | +1 | +2 | +3 | +4 | |||||||||
| สังกะสี | Zn | +1 | +2 | [7] | ||||||||||
| แกลเลียม | Ga | +1 | +2 | +3 | ||||||||||
| เจอร์เมเนียม | −4 | −3 | −2 | −1 | Ge | +1 | +2 | +3 | +4 | [8] | ||||
| สารหนู | −3 | As | +1 | +2 | +3 | +5 | [9] | |||||||
| ซีลีเนียม | −2 | Se | +1 | +2 | +4 | +6 | [10] | |||||||
| โบรมีน | −1 | Br | +1 | +2 | +3 | +4 | +5 | +7 | ||||||
| คริปทอน | Kr | +2 | ||||||||||||
| รูบิเดียม | −1 | Rb | +1 | |||||||||||
| สตรอนเชียม | Sr | +1 | +2 | [11] | ||||||||||
| อิตเทรียม | Y | +1 | +2 | +3 | [12][13] | |||||||||
| เซอร์โคเนียม | Zr | +1 | +2 | +3 | +4 | |||||||||
| ไนโอเบียม | −1 | Nb | +1 | +2 | +3 | +4 | +5 | [14] | ||||||
| โมลิบดีนัม | −2 | −1 | Mo | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| เทคนีเชียม | −3 | −1 | Tc | +1 | +2 | +3 | +4 | +5 | +6 | +7 | ||||
| รูทีเนียม | −2 | Ru | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | ||||
| โรเดียม | −1 | Rh | +1 | +2 | +3 | +4 | +5 | +6 | ||||||
| แพลเลเดียม | Pd | +1 | +2 | +4 | [15] | |||||||||
| เงิน | Ag | +1 | +2 | +3 | +4 | [16] | ||||||||
| แคดเมียม | Cd | +1 | +2 | [17] | ||||||||||
| อินเดียม | In | +1 | +2 | +3 | ||||||||||
| ดีบุก | −4 | Sn | +2 | +4 | ||||||||||
| พลวง | −3 | Sb | +3 | +5 | ||||||||||
| เทลลูเรียม | −2 | Te | +2 | +4 | +5 | +6 | ||||||||
| ไอโอดีน | −1 | I | +1 | +3 | +4 | +5 | +7 | [18] | ||||||
| ซีนอน | Xe | +1 | +2 | +4 | +6 | +8 | [19] | |||||||
| ซีเซียม | −1 | Cs | +1 | |||||||||||
| แบเรียม | Ba | +2 | ||||||||||||
| แลนทานัม | La | +2 | +3 | |||||||||||
| ซีเรียม | Ce | +2 | +3 | +4 | ||||||||||
| เพรซีโอดิเมียม | Pr | +2 | +3 | +4 | ||||||||||
| นีโอดิเมียม | Nd | +2 | +3 | +4 | [20] | |||||||||
| โพรมีเทียม | Pm | +2 | +3 | [21] | ||||||||||
| ซาแมเรียม | Sm | +2 | +3 | |||||||||||
| ยูโรเพียม | Eu | +2 | +3 | |||||||||||
| แกโดลิเนียม | Gd | +1 | +2 | +3 | ||||||||||
| เทอร์เบียม | Tb | +1 | +2 | +3 | +4 | [22] | ||||||||
| ดิสโพรเซียม | Dy | +2 | +3 | +4 | [23] | |||||||||
| โฮลเมียม | Ho | +2 | +3 | [24] | ||||||||||
| เออร์เบียม | Er | +2 | +3 | [25] | ||||||||||
| ทูเลียม | Tm | +2 | +3 | +4 | [26] | |||||||||
| อิตเทอร์เบียม | Yb | +2 | +3 | |||||||||||
| ลูทีเชียม | Lu | +3 | ||||||||||||
| ฮาฟเนียม | Hf | +2 | +3 | +4 | ||||||||||
| แทนทาลัม | −1 | Ta | +2 | +3 | +4 | +5 | ||||||||
| ทังสเตน | −2 | −1 | W | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| รีเนียม | −3 | −1 | Re | +1 | +2 | +3 | +4 | +5 | +6 | +7 | ||||
| ออสเมียม | −2 | −1 | Os | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | [27] | ||
| อิริเดียม | −3 | −1 | Ir | +1 | +2 | +3 | +4 | +5 | +6 | +8 | [28][29] | |||
| แพลตทินัม | −2 | −1 | Pt | +1 | +2 | +3 | +4 | +5 | +6 | [30][31] | ||||
| ทองคำ | −1 | Au | +1 | +2 | +3 | +5 | ||||||||
| ปรอท | Hg | +1 | +2 | +4 | [32] | |||||||||
| แทลเลียม | −1 | Tl | +1 | +3 | [33] | |||||||||
| ตะกั่ว | −4 | Pb | +2 | +4 | ||||||||||
| บิสมัท | −3 | Bi | +1 | +3 | +5 | [34] | ||||||||
| พอโลเนียม | −2 | Po | +2 | +4 | +5 | +6 | [35] | |||||||
| แอสทาทีน | −1 | At | +1 | +3 | +5 | +7 | ||||||||
| เรดอน | Rn | +2 | +6 | [36][37][38] | ||||||||||
| แฟรนเซียม | Fr | +1 | ||||||||||||
| เรเดียม | Ra | +2 | ||||||||||||
| แอกทิเนียม | Ac | +2 | +3 | [39] | ||||||||||
| ทอเรียม | Th | +2 | +3 | +4 | ||||||||||
| โพรแทกทิเนียม | Pa | +2 | +3 | +4 | +5 | [40] | ||||||||
| ยูเรเนียม | U | +2 | +3 | +4 | +5 | +6 | [41] | |||||||
| เนปทูเนียม | Np | +3 | +4 | +5 | +6 | +7 | ||||||||
| พลูโทเนียม | Pu | +3 | +4 | +5 | +6 | +7 | +8 | [42] | ||||||
| อะเมริเซียม | Am | +2 | +3 | +4 | +5 | +6 | +7 | [43] | ||||||
| คูเรียม | Cm | +2 | +3 | +4 | [44] | |||||||||
| เบอร์คีเลียม | Bk | +2 | +3 | +4 | [45] | |||||||||
| แคลิฟอร์เนียม | Cf | +2 | +3 | +4 | ||||||||||
| ไอน์สไตเนียม | Es | +2 | +3 | +4 | [46] | |||||||||
| เฟอร์เมียม | Fm | +2 | +3 | |||||||||||
| เมนเดลีเวียม | Md | +2 | +3 | |||||||||||
| โนเบเลียม | No | +2 | +3 | |||||||||||
| ลอว์เรนเซียม | Lr | +3 | ||||||||||||
| รัทเทอร์ฟอร์เดียม | Rf | +4 | ||||||||||||
| ดุบเนียม | Db | +5 | [47] | |||||||||||
| ซีบอร์เกียม | Sg | +6 | [48] | |||||||||||
| โบห์เรียม | Bh | +7 | [49] | |||||||||||
| ฮาสเซียม | Hs | +8 | [50] | |||||||||||
| ไมต์เนเรียม | Mt | +3 | +4 | [ต้องการอ้างอิง] | ||||||||||
| ดาร์มสตัดเทียม | Ds | +3 | +4 | [ต้องการอ้างอิง] | ||||||||||
| เรินต์เกเนียม | Rg | +3 | [ต้องการอ้างอิง] | |||||||||||
| โคเปอร์นิเซียม | Cn | +1 | +2 | [ต้องการอ้างอิง] | ||||||||||
| นิโฮเนียม | Nh | +1 | +3 | [ต้องการอ้างอิง] | ||||||||||
| ฟลีโรเวียม | Fl | +2 | [ต้องการอ้างอิง] | |||||||||||
| มอสโกเวียม | Mc | +3 | +5 | [ต้องการอ้างอิง] | ||||||||||
| ลิเวอร์มอเรียม | Lv | +4 | +5 | [ต้องการอ้างอิง] | ||||||||||
| เทนเนสซีน | −1 | Ts | +1 | +3 | +5 | +7 | [ต้องการอ้างอิง] | |||||||
| ออกาเนสซอน | Og | +2 | [ต้องการอ้างอิง] | |||||||||||
| อูนอูนเอนเนียม | Uue | +1 | [ต้องการอ้างอิง] | |||||||||||
| อูนไบนิลเลียม | Ubn | +2 | [ต้องการอ้างอิง] | |||||||||||
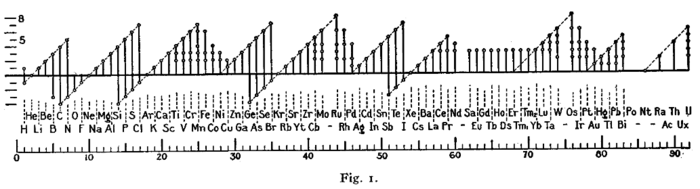
รูปที่แสดงด้านล่างนี้เป็นรูปที่ถูกใช้โดย เออร์วิง แลงเมียร์ในปี 2462 โดยเป็นแผ่นกระดาษที่เกี่ยวกับกฎออกเตต[51] The periodicity of the oxidation states was one of the pieces of evidence that led Langmuir to adopt the rule.
รายการอ้างอิง
[แก้]- ↑ Be(I) ถูกพบใน เบริลเลียม มอโนไฮไดรต์ (BeH); see "Beryllium: Beryllium(I) Hydride compound data" (PDF). bernath.uwaterloo.ca. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2007-12-02. สืบค้นเมื่อ 2007-12-10.
- ↑ Low valent magnesium compounds with Mg(I) have been obtained using bulky ligands; see Green, S. P.; Jones C.; Stasch A. (December 2007). "Stable Magnesium(I) Compounds with Mg-Mg Bonds". Science. 318 (5857): 1754–1757. Bibcode:2007Sci...318.1754G. doi:10.1126/science.1150856. PMID 17991827. S2CID 40657565.
- ↑ Al(II) has been observed in aluminium(II) oxide (AlO); see D. C. Tyte (1964). "Red (B2Π–A2σ) Band System of Aluminium Monoxide". Nature. 202 (4930): 383. Bibcode:1964Natur.202..383T. doi:10.1038/202383a0., and in dialanes (R2Al—AlR2); see Uhl, Werner "Organoelement Compounds Possessing Al—Al, Ga—Ga, In—In, and Tl—Tl Single Bonds" Advances in Organometallic Chemistry Volume 51, 2004, Pages 53–108. doi:10.1016/S0065-3055(03)51002-4
- ↑ Ca(I) has been observed; see Krieck, Sven; Görls, Helmar; Westerhausen, Matthias (2010). "Mechanistic Elucidation of the Formation of the Inverse Ca(I) Sandwich Complex [(thf)3Ca(μ-C6H3-1,3,5-Ph3)Ca(thf)3] and Stability of Aryl-Substituted Phenylcalcium Complexes". Journal of the American Chemical Society. 132 (35): 12492–501. doi:10.1021/ja105534w. PMID 20718434.
- ↑ Ti(I) has been observed in [Ti(η6-1,3,5-C6H3iPr3)2][BAr4] (Ar = C6H5, p-C6H4F, 3,5-C6H3(CF3)2); see Calderazzo, Fausto; Ferri, Isabella; Pampaloni, Guido; Englert, Ulli; Green, Malcolm L. H. (1997). "Synthesis of [Ti(η6-1,3,5-C6H3iPr3)2][BAr4] (Ar = C6H5, p-C6H4F, 3,5-C6H3(CF3)2), the First Titanium(I) Derivatives". Organometallics. 16 (14): 3100–3101. doi:10.1021/om970155o.
- ↑ Fe(VII) and Fe(VIII) have been reported; see Yurii D. Perfiliev; Virender K. Sharma (2008). "เลขออกซิเดชันที่สูงของเหล็กในสถานะของแข็ง: Synthesis and Their Mössbauer Characterization – Ferrates – ACS Symposium Series (ACS Publications)". Platinum Metals Review. 48 (4): 157. doi:10.1595/147106704X10801. However, their existence has been disputed.
- ↑ Zn(I) has been observed in Zn2Cl2; see Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Zink". Lehrbuch der Anorganischen Chemie (ภาษาเยอรมัน) (91–100 ed.). Walter de Gruyter. pp. 1034–1041. ISBN 3-11-007511-3.
- ↑ Ge(−1), Ge(−2), and Ge(−3) have been observed in germanes; see Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8..
- ↑ As(I) has been observed in arsenic(I) iodide (AsI); see Ellis, Bobby D.; MacDonald, Charles L. B. (2004). "Stabilized Arsenic(I) Iodide: A Ready Source of Arsenic Iodide Fragments and a Useful Reagent for the Generation of Clusters". Inorganic Chemistry. 43 (19): 5981–6. doi:10.1021/ic049281s. PMID 15360247.
- ↑ Se(I) has been observed in selenium(I) chloride (Se2Cl2); see "Selenium : Selenium(I) chloride compound data". WebElements.com. สืบค้นเมื่อ 2007-12-10.
- ↑ Sr(I) has been observed in strontium monofluoride (SrF); see P. Colarusso; Guo, B.; Zhang, K.-Q.; Bernath, P.F.; และคณะ (1996). "High-Resolution Infrared Emission Spectrum of Strontium Monofluoride" (PDF). Journal of Molecular Spectroscopy. 175 (1): 158–171. Bibcode:1996JMoSp.175..158C. doi:10.1006/jmsp.1996.0019. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2012-03-08.
- ↑ Y(I) has been observed in yttrium(I) bromide (YBr); see "Yttrium: yttrium(I) bromide compound data". OpenMOPAC.net. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-07-23. สืบค้นเมื่อ 2007-12-10.
- ↑ Y(II) has been observed in yttrium(II) hydride (YH2); see "Yttrium: yttrium(II) hydride compound data". WebElements.com. สืบค้นเมื่อ 2007-12-10.
- ↑ Nb(I) has been observed in niobium monochloride (NbCl); see Ram, R.S.; Rinskopf, N.; Liévin, J.; Bernatha, P.F. (2004). "Fourier transform emission spectroscopy and ab initio calculations on NbCl" (PDF). Journal of Molecular Spectroscopy. 228 (2): 544–553. Bibcode:2004JMoSp.228..544R. doi:10.1016/j.jms.2004.02.001. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2014-02-28.
- ↑ Pd(I) has been observed; see Crabtree, R. H. (2002). "CHEMISTRY: A New Oxidation State for Pd?". Science. 295 (5553): 288. doi:10.1126/science.1067921.
- ↑ Ag(IV) has been observed in potassium hexafluoroargentate (K2AgF6) and caesium hexafluoroargentate (Cs2AgF6); see Riedel, Sebastian; Kaupp, Martin (2009). "The highest oxidation states of the transition metal elements" (PDF). Coordination Chemistry Reviews. Elsevier. 253: 606–624.
- ↑ Cd(I) has been observed in cadmium(I) tetrachloroaluminate (Cd2(AlCl4)2); see Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Cadmium". Lehrbuch der Anorganischen Chemie (ภาษาเยอรมัน) (91–100 ed.). Walter de Gruyter. pp. 1056–1057. ISBN 978-3-11-007511-3.
- ↑ I(IV) has been observed in iodine dioxide (IO2); see Pauling, Linus (1988). "Oxygen Compounds of Nonmetallic Elements". General Chemistry (3rd ed.). Dover Publications, Inc. pp. 259. ISBN 0-486-65622-5.
- ↑ Xe(I) has been observed in xenon hexafluoroplatinate and xenon hexafluororhodate; see Pauling, Linus (1988). General Chemistry (3rd ed.). Dover Publications, Inc. pp. 250. ISBN 0-486-65622-5.
- ↑ Nd(IV) has been observed in unstable solid state compounds; see แม่แบบ:Holleman&Wiberg
- ↑ Pm(II) has been observed in dilute, solid solutions of promethium dihalides in alkaline earth dihalides; see แม่แบบ:Holleman&Wiberg
- ↑ Tb(II) has been observed in terbium dihydride (TbH2), terbium(II) selenide (TbSe), and terbium(II) telluride (TbTe); see Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. pp. 920–921. ISBN 0-07-049439-8. สืบค้นเมื่อ 2009-06-06.
- ↑ Dy(IV) has been observed in unstable solid state compounds; see แม่แบบ:Holleman&Wiberg
- ↑ Ho(II) has been observed in dilute, solid solutions of holmium dihalides in alkaline earth dihalides; see แม่แบบ:Holleman&Wiberg
- ↑ Er(II) has been observed in dilute, solid solutions of erbium dihalides in alkaline earth dihalides; see แม่แบบ:Holleman&Wiberg
- ↑ Tm(IV) has been observed; see Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. p. 934. ISBN 0-07-049439-8. สืบค้นเมื่อ 2009-06-06.
- ↑ Os(−1) has been observed in Na[Os(CO)
13]; see Krause, J.; Siriwardane, Upali; Salupo, Terese A.; Wermer, Joseph R.; Knoeppel, David W.; Shore, Sheldon G. (1993). "Preparation of [Os3(CO)11]2− and its reactions with Os3(CO)12; structures of [Et4N] [HOs3(CO)11] and H2OsS4(CO)". Journal of Organometallic Chemistry. 454 (1–2): 263–271. doi:10.1016/0022-328X(93)83250-Y. and Carter, Willie J.; Kelland, John W.; Okrasinski, Stanley J.; Warner, Keith E.; Norton, Jack R. (1982). "Mononuclear hydrido alkyl carbonyl complexes of osmium and their polynuclear derivatives". Inorganic Chemistry. 21 (11): 3955–3960. doi:10.1021/ic00141a019. - ↑ Ir(−3) has been observed in Ir(CO)33−; see Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 1117. ISBN 978-0-08-037941-8.
- ↑ Ir(VIII) has been observed in iridium tetroxide (IrO4); see Gong, Yu; Zhou, Mingfei; Kaupp, Martin; Riedel, Sebastian (2009). "Formation and Characterization of the Iridium Tetroxide Molecule with Iridium in the Oxidation State +VIII". Angewandte Chemie International Edition. 48 (42): 7879. doi:10.1002/anie.200902733.
- ↑ Pt(−1) and Pt(−2) have been observed in the barium platinides Ba2Pt, BaPt, and Ba3Pt2 respectively: see Karpov, Andrey; Konuma, Mitsuharu; Jansen, Martin (2006). "An experimental proof for negative oxidation states of platinum: ESCA-measurements on barium platinides". Chemical Communications (8): 838–840. doi:10.1039/b514631c. PMID 16479284.
- ↑ Pt(I) and Pt(III) have been observed in bimetallic and polymetallic species; see Kauffman, George B.; Thurner, Joseph J.; Zatko, David A. (1967). "Ammonium Hexachloroplatinate(IV)". Inorganic Syntheses. Inorganic Syntheses. 9: 182–185. doi:10.1002/9780470132401.ch51. ISBN 978-0-470-13240-1.
- ↑ Hg(IV) has been reported in mercury(IV) fluoride (HgF4); see Xuefang Wang; Lester Andrews; Sebastian Riedel; Martin Kaupp (2007). "Mercury Is a Transition Metal: The First Experimental Evidence for HgF4". Angew. Chem. Int. Ed. 46 (44): 8371–8375. doi:10.1002/anie.200703710. PMID 17899620. However, it could not be confirmed by later experiments; see Is mercury a transition metal? เก็บถาวร 2016-10-12 ที่ เวย์แบ็กแมชชีน
- ↑ Tl(−1) has been observed in caesium thallide (CsTl); see Bashilova NI & Khomutova, TV 1984, ‘Thallates of alkali metals and monovalent thallium formed in aqueous solutions of their hydroxides’, Russian Chemical Bulletin, vol. 33, no. 8, August, pp. 1543–47.
- ↑ Bi(I) has been observed in bismuth monobromide (BiBr) and bismuth monoiodide (BiI); see Godfrey, S. M.; McAuliffe, C. A.; Mackie, A. G.; Pritchard, R. G. (1998). Nicholas C. Norman (บ.ก.). Chemistry of arsenic, antimony, and bismuth. Springer. pp. 67–84. ISBN 0-7514-0389-X.
- ↑ Po(V) has been observed in dioxidopolonium(1+) (PoO+
2); see Thayer, John S. (2010). Chemistry of heavier main group elements. p. 78. doi:10.1007/9781402099755_2. - ↑ Rn(II) has been observed in radon difluoride (RnF2); see Stein, L. (1970). "Ionic Radon Solution". Science. 168 (3929): 362–4. Bibcode:1970Sci...168..362S. doi:10.1126/science.168.3929.362. PMID 17809133. and Kenneth S. Pitzer (1975). "Fluorides of radon and element 118". J. Chem. Soc., Chem. Commun., (18): 760b–761. doi:10.1039/C3975000760b.
{{cite journal}}: CS1 maint: extra punctuation (ลิงก์) - ↑ Rn(IV) is reported by Greenwood and Earnshaw, but is not known to exist; see Sykes, A. G. (1998). "Recent Advances in Noble-Gas Chemistry". Advances in Inorganic Chemistry. Vol. 46. Academic Press. pp. 91–93. ISBN 978-0120236466. สืบค้นเมื่อ 22 November 2012.
- ↑ Rn(VI) is known in radon trioxide (RnO3); see Sykes, A. G. (1998). "Recent Advances in Noble-Gas Chemistry". Advances in Inorganic Chemistry. Vol. 46. Academic Press. pp. 91–93. ISBN 978-0120236466. สืบค้นเมื่อ 22 November 2012.
- ↑ Ac(II) is known in actinium dihydride (AcH2); see Farr, J (1961). "The crystal structure of actinium metal and actinium hydride". Journal of Inorganic and Nuclear Chemistry. 18: 42. doi:10.1016/0022-1902(61)80369-2.
- ↑ Pa(II) is known in protactinium(II) oxide (PaO); see Sellers, Philip A.; Fried, Sherman; Elson, Robert E.; Zachariasen, W. H. (1954). "The Preparation of Some Protactinium Compounds and the Metal". Journal of the American Chemical Society. 76 (23): 5935. doi:10.1021/ja01652a011.
- ↑ U(II) has been observed in uranium monoxide (UO), uranium monosulfide (US), uranium acetylide (UC2), and uranium sesquicarbide (U2C3); see A.L. Bowman, G.P. Arnold, W.G. Witteman, T.C. Wallace and N.G. Nereson, Acta Crystallographica, 1966, 21, 670–671.
- ↑ Unstable Pu(VIII) complexes can form in alkaline solutions; see Kiselev, Yu. M.; Nikonov, M. V.; Tananaev, I. G.; Myasoedov, B. F. (2009). "On the Existence of Plutonium Tetroxide". Doklady Akademii Nauk. Pleiades Publishing, Ltd. 425 (5): 634–637. doi:10.1134/S0012501609040022. ISSN 0012-5016. สืบค้นเมื่อ February 25, 2012.[ลิงก์เสีย]
- ↑ Am(VII) has been observed in AmO5−
6; see Americium, Das Periodensystem der Elemente für den Schulgebrauch (The periodic table of elements for schools) chemie-master.de (in German), Retrieved 28 November 2010 and Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 1265. ISBN 978-0-08-037941-8. - ↑ Cm(II) has been observed in curium(II) oxide (CmO2); see Holleman, Arnold F. and Wiberg, Nils Textbook of Inorganic Chemistry, p.1972, 102 Edition, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Bk(II) has been observed in berkelium(II) oxide (BkO); see Peterson J. R. and Hobart D. E. "The Chemistry of Berkelium" in Harry Julius Emeléus (Ed.) Advances in inorganic chemistry and radiochemistry, Volume 28, Academic Press, 1984 ISBN 0-12-023628-1, p. 51, doi:10.1016/S0898-8838(08)60204-4
- ↑ Es(IV) is known in einsteinium(IV) fluoride (EsF4); see Kleinschmidt, P (1994). "Thermochemistry of the actinides". Journal of Alloys and Compounds. 213–214: 169. doi:10.1016/0925-8388(94)90898-2.
- ↑ Db(V) has been observed in dubnium pentachloride (DbCl5); see H. W. Gäggeler (2007). "Gas Phase Chemistry of Superheavy Elements" (PDF). Paul Scherrer Institute. pp. 26–28. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2012-02-20. สืบค้นเมื่อ 2021-11-02.
- ↑ Sg(VI) has been observed in seaborgium oxide hydroxide (SgO2(OH)2); see Huebener, S.; Taut, S.; Vahle, A.; Dressler, R.; Eichler, B.; Gäggeler, H. W.; Jost, D.T.; Piguet, D.; และคณะ (2001). "Physico-chemical characterization of seaborgium as oxide hydroxide" (PDF). Radiochim. Acta. 89 (11–12_2001): 737–741. doi:10.1524/ract.2001.89.11-12.737. S2CID 98583998. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2014-10-25.
- ↑ Bh(VII) has been observed in bohrium oxychloride (BhO3Cl); see "Gas chemical investigation of bohrium (Bh, element 107)" เก็บถาวร 2008-02-28 ที่ เวย์แบ็กแมชชีน, Eichler et al., GSI Annual Report 2000. Retrieved on 2008-02-29
- ↑ Hs(VIII) has been observed in hassium tetroxide (HsO4); see "Chemistry of Hassium" (PDF). Gesellschaft für Schwerionenforschung mbH. 2002. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2012-01-14. สืบค้นเมื่อ 2007-01-31.
- ↑ Langmuir, Irving (1919). "The arrangement of electrons in atoms and molecules". J. Am. Chem. Soc. 41 (6): 868–934. doi:10.1021/ja02227a002.