ด่างทับทิม
หน้าตา
| |

| |

| |
| ชื่อ | |
|---|---|
| IUPAC name
Potassium manganate(VII)
| |
| Systematic IUPAC name
Potassium permanganate | |
| ชื่ออื่น
Chameleon mineral
Condy's crystals Permanganate of potash Hypermangan Purple potion powder | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| ChEMBL | |
| เคมสไปเดอร์ | |
| ดรักแบงก์ | |
| ECHA InfoCard | 100.028.874 |
| EC Number |
|
| KEGG | |
ผับเคม CID
|
|
| RTECS number |
|
| UNII | |
| UN number | 1490 |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| KMnO4 | |
| มวลโมเลกุล | 158.034 g/mol |
| ลักษณะทางกายภาพ | Purplish-bronze-gray needles purple in solution[1] |
| กลิ่น | odorless |
| ความหนาแน่น | 2.7 g/cm3[2]: 4.83 |
| จุดหลอมเหลว | 240 องศาเซลเซียส (464 องศาฟาเรนไฮต์; 513 เคลวิน) (decomposes) |
| 76 g/L (25 °C)[2] 250 g/L (65 °C) | |
| ความสามารถละลายได้ | decomposes in alcohol and organic solvents |
| +20.0·10−6 cm3/mol[2]: 4.134 | |
ดัชนีหักเหแสง (nD)
|
1.59 |
| โครงสร้าง[3] | |
| Orthorhombic, oP24 | |
| Pnma, No. 62 | |
a = 0.909 nm, b = 0.572 nm, c = 0.741 nm
| |
หน่วยสูตร (Z)
|
4 |
| อุณหเคมี | |
ความจุความร้อน (C)
|
119.2 J/mol K |
Std molar
entropy (S⦵298) |
171.7 J K−1 mol−1 |
Std enthalpy of
formation (ΔfH⦵298) |
−813.4 kJ/mol |
พลังงานเสรีกิบส์ (ΔfG⦵)
|
-713.8 kJ/mol |
| เภสัชวิทยา | |
| D08AX06 (WHO) V03AB18 | |
| ความอันตราย | |
| GHS labelling: | |
  
| |
| NFPA 704 (fire diamond) | |
| ปริมาณหรือความเข้มข้น (LD, LC): | |
LD50 (median dose)
|
1090 mg/kg (oral, rat)[4] |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
แอนไอออนอื่น ๆ
|
Potassium pertechnetate Potassium perrhenate |
แคทไอออนอื่น ๆ
|
Sodium permanganate Ammonium permanganate Calcium permanganate Silver permanganate |
manganatesที่เกี่ยวข้อง
|
Potassium hypomanganate Potassium manganate |
สารประกอบที่เกี่ยวข้อง
|
Manganese heptoxide |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
| ข้อมูลทางคลินิก | |
|---|---|
| ข้อมูลทะเบียนยา | |
| ตัวบ่งชี้ | |
| ECHA InfoCard | 100.028.874 |
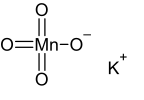
ด่างทับทิม มีชื่อทางเคมีว่า โพแทสเซียมเปอร์แมงกาเนต (KMnO4) มีลักษณะเป็นผลึกสีม่วง ใช้ในการแช่ผักหรือผลไม้เพื่อชะล้างสารเคมี เป็นสารประกอบประเภทเกลือ มีฤทธิ์เป็นเบสอ่อนๆ
อ้างอิง
[แก้]- ↑ Burriel F, Lucena F, Arribas S, Hernández J (1985). Química Analítica Cualitativa [Qualitative Analytical Chemistry] (ภาษาสเปน). Ediciones Paraninfo, S.A. p. 688. ISBN 84-9732-140-5.
- ↑ 2.0 2.1 2.2 Haynes WM, บ.ก. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
- ↑ Hocart R, Mathieu-Sicaud A (1945). "A stabilization factor in the polymorphism of ammonium nitrate". Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences [Weekly Reports of the Sessions of the Academy of Sciences] (ภาษาฝรั่งเศส). 221: 261–263.
- ↑ Chambers M. "Potassium permanganate [USP:JAN] – Similar structures search, synonyms, formulas, resource links, and other chemical information". ChemIDplus: A Toxnet database. U.S. National Library of Medicine. ChemIDplus – CAS: 7722-64-7 InChi: VZJVWSHVAAUDKD-UHFFFAOYSA-N. เก็บจากแหล่งเดิมเมื่อ 13 August 2014. สืบค้นเมื่อ 9 May 2018.
อ่านเพิ่มเติม
[แก้]- "Potassium permanganate". Drug Information Portal. U.S. National Library of Medicine.
- "Manganese and compounds Fact Sheet". National Pollutant Inventory. Australia: Department of Climate Change, Energy, the Environment and Water.
- Lazur AM (2009). "The use of potassium permanganate in fish ponds". IFAS Extention. Gainesville, FL: University of Florida. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-06-06.

